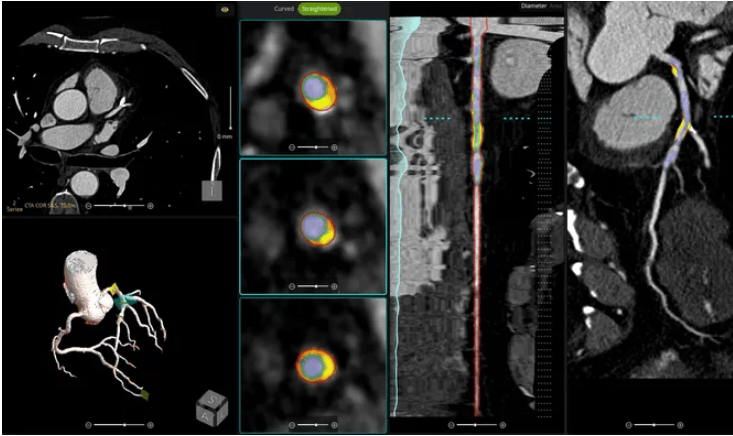
Paris, le 18 mars 2026 — L'Administration américaine des denrées alimentaires et des médicaments (FDA) a accordé la désignation de thérapie révolutionnaire à venglustat, un médicament de Sanofi. Il s'agit d'un nouvel inhibiteur oral de la glucosylcéramide synthase (GCSi), destiné au traitement des manifestations neurologiques de la maladie de Gaucher de type 3 (GD3). La maladie de Gaucher est une maladie lysosomale rare, et cette désignation repose sur les données positives de l'essai clinique de phase 3 LEAP2MONO.
Dans l'étude LEAP2MONO, venglustat a montré un avantage statistiquement significatif par rapport aux patients sous enzymothérapie substitutive (ERT) pour améliorer les symptômes neurologiques, mesuré par un score composite évaluant l'ataxie et la cognition. Le médicament a été bien toléré, avec des événements indésirables fréquents incluant maux de tête, nausées, etc. La maladie de Gaucher est causée par un déficit en glucocérébrosidase, entraînant une accumulation de glycosphingolipides (GSL) dans les organes. Le type 3 implique une atteinte du système nerveux central, et il n'existe actuellement aucun traitement approuvé ciblant spécifiquement ses symptômes neurologiques.
Karin Knobe, responsable mondiale du développement clinique des maladies rares chez Sanofi, a déclaré : « Ce jalon réglementaire reconnaît le besoin médical important et non satisfait des patients atteints de la maladie de Gaucher de type 3, en particulier ceux qui subissent une détérioration neurologique progressive. Les résultats positifs de l'étude LEAP2MONO constituent une étape encourageante dans le processus de développement, et nous continuerons de collaborer avec la FDA pour faire avancer cette option thérapeutique potentielle. » Venglustat est conçu pour traverser la barrière hémato-encéphalique et cibler le mécanisme pathologique de l'accumulation anormale de GSL, afin de ralentir la progression de la maladie.
Précédemment, venglustat avait obtenu la désignation de voie accélérée de la FDA, ainsi que les désignations de médicament orphelin aux États-Unis, dans l'Union européenne et au Japon. Sanofi prévoit de soumettre des demandes d'autorisation réglementaire mondiales pour l'utilisation du médicament dans la maladie de Gaucher de type 3 en 2026. La désignation de thérapie révolutionnaire de la FDA vise à accélérer le développement et l'examen des médicaments pour des maladies graves, exigeant que le médicament montre un potentiel supérieur aux traitements existants sur des critères d'évaluation cliniquement significatifs.