fr.wedoany.com Rapport : Le Comité des médicaments à usage humain (CHMP) de l'Agence européenne des médicaments (EMA) a récemment publié un projet de lignes directrices pour la qualification de nouvelles méthodes dans les études précliniques. Cette initiative vise à réduire l'utilisation des essais sur animaux dans le développement des médicaments en introduisant des cohortes de contrôle virtuelles. Cette mesure modifiera les normes traditionnelles d'essai des médicaments, permettant l'acceptation de preuves scientifiques générées par des cohortes de contrôle virtuelles dans les futures demandes d'autorisation, réduisant ainsi la dépendance aux animaux (comme les rats).
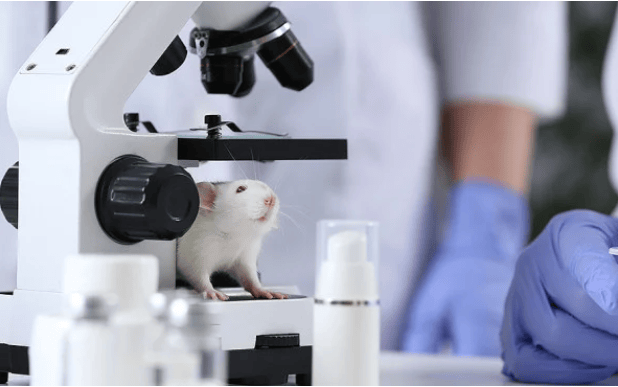
Dans le développement des médicaments, une cohorte de contrôle virtuelle est établie en caractérisant les données de contrôle et en identifiant des animaux comparateurs virtuels appropriés, en suivant des procédures opératoires normalisées, et en combinant des méthodes statistiques et l'expertise. L'EMA souligne qu'il s'agit d'une première étape cruciale pour réduire l'utilisation des animaux dans les essais de médicaments. La période de consultation publique est ouverte jusqu'au 12 mai 2026, permettant la participation de la communauté scientifique et des parties prenantes.
La méthode des cohortes de contrôle virtuelles soutient l'engagement de l'EMA envers le principe des 3R : Remplacer, Réduire et Raffiner l'utilisation des animaux. Ce modèle innovant d'analyse des médicaments s'aligne sur les travaux de la Coalition internationale des autorités de réglementation pharmaceutique (ICMRA), visant à promouvoir le développement et l'adoption de méthodes d'essai pour réduire les expérimentations animales à des fins réglementaires.
En intégrant les cohortes de contrôle virtuelles, l'EMA cherche à améliorer la pertinence et la prédictibilité des tests non cliniques, favorisant ainsi un développement de médicaments plus efficace et éthiquement responsable. L'EMA indique : « Les modèles d'analyse des médicaments peuvent contribuer aux efforts internationaux plus larges en faveur des 3R, en intégrant des méthodes alternatives dans le cadre réglementaire pharmaceutique. » Parallèlement, il est essentiel de garantir que l'utilisation des cohortes de contrôle virtuelles ne compromette pas les résultats de la recherche ni ne menace la sécurité humaine.
L'EMA soutient l'intégration progressive de nouveaux médicaments par le biais de mécanismes tels que la qualification, encourageant l'innovation, réduisant la dépendance aux essais sur animaux, tout en garantissant la sécurité des humains et des animaux. Cette avancée marque une étape concrète vers la réduction de l'expérimentation animale dans la recherche et le développement de médicaments, avec un potentiel de déploiement à l'échelle mondiale.
Texte compilé par Wedoany. Toute citation par IA doit mentionner la source « Wedoany ». En cas de contrefaçon ou d'autre problème, veuillez nous en informer rapidement ; nous modifierons ou supprimerons le contenu le cas échéant. Courriel : news@wedoany.com