fr.wedoany.com Rapport : Une équipe de recherche européenne a récemment publié une étude dans la revue Crystals, explorant l'application d'enzymes thermostables dans le recyclage du polyéthylène téréphtalate (PET). Le PET est largement utilisé dans les emballages et les textiles, et son processus de recyclage nécessite généralement des technologies de dépolymérisation efficaces. L'étude montre qu'à des températures proches de 70 °C, le polymère PET devient plus accessible, permettant ainsi une dépolymérisation efficace. Dans ces conditions, l'enzyme doit conserver son intégrité structurelle et la flexibilité de son site actif, une combinaison qui représente un défi pour la conception enzymatique.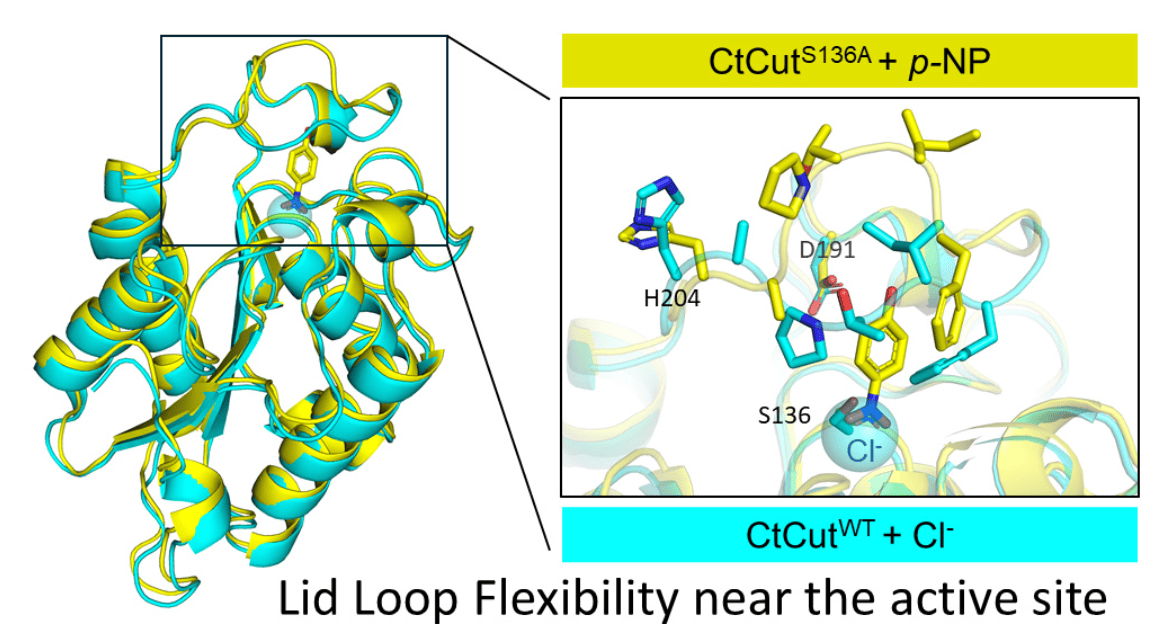
L'équipe de recherche a analysé la cutinase dérivée de Chaetomium thermophilum, incluant l'enzyme naturelle (CtCutWT) et un variant mutant (CtCutS136A). La caractérisation structurelle et les mesures de stabilité thermique ont été effectuées par calorimétrie différentielle à balayage, dans une plage de températures de 30 °C à 100 °C. Cette enzyme adopte un repliement α/β-hydrolase, formant un cadre stable, tandis qu'une boucle mobile en forme de couvercle recouvre le site actif, régulant l'accès au substrat. Les observations structurelles indiquent que cette boucle subit un changement conformationnel lors de la liaison du ligand, ce qui contribue à la fonction catalytique sans affecter la stabilité globale.
Un ion chlorure a été détecté à proximité du site actif, indiquant la présence d'un microenvironnement chargé positivement, ce qui pourrait favoriser les interactions avec le substrat. L'analyse thermique a révélé un processus de dépliement en deux étapes : des changements structurels initiaux commençant vers 60 °C, et une deuxième transition se produisant entre 65 °C et 70 °C. Ces résultats soutiennent l'idée que différentes régions de l'enzyme possèdent des stabilités thermiques distinctes, illustrant le concept de compartimentation fonctionnelle des protéines.
Les résultats de l'étude suggèrent qu'une enzyme efficace pour le recyclage biologique du PET pourrait nécessiter de combiner un cœur structurel stable avec une flexibilité locale au niveau de l'interface catalytique. Cette conception structurelle permet à la fois de supporter la thermostabilité et d'améliorer l'adaptabilité au substrat, fournissant une base pour le développement d'enzymes améliorées destinées au recyclage industriel des plastiques. L'étude a été publiée le 24 mars 2026 dans la revue Crystals (Volume 16, Numéro spécial 4) et pourrait potentiellement contribuer au développement des technologies de recyclage des plastiques à l'échelle mondiale.
Texte compilé par Wedoany. Toute citation par IA doit mentionner la source « Wedoany ». En cas de contrefaçon ou d'autre problème, veuillez nous en informer rapidement ; nous modifierons ou supprimerons le contenu le cas échéant. Courriel : news@wedoany.com